肺炎是全球范围内导致死亡和致残的重要疾病之一。尽管抗生素和抗炎药物的应用在过去几十年里挽救了无数生命,但这些传统疗法普遍存在药物靶向性差、耐药性逐渐增加以及无法有效调控肺部炎症微环境等问题。这些局限性使得临床上对于重症肺炎,尤其是伴随细胞因子风暴的病例,仍缺乏精准而有效的干预手段。理想的治疗方式需要具备主动靶向感染或炎症病灶、中和关键炎症因子、实现药物长效滞留并能重新塑造局部免疫微环境的综合能力。
近日,南方医科大学涂盈锋团队与中山大学彭飞团队合作在 Nature Communications 发表的一项研究“Biomimetic magnetobacterial microrobots for active pneumonia therapy”,提出了一种基于合成生物学与微纳机器人技术的创新策略。他们开发出一种仿生磁细菌微型机器人(Active Robot,AR),通过细胞膜伪装、药物负载与化学组装,将自然界的磁驱细菌改造为多功能治疗平台。这一系统能够在外部磁场控制下主动运动,实现对病毒及炎症因子的清除、药物的精准递送以及免疫环境的重塑,为肺炎治疗提供了一条全新的路径。

研究团队首先在设计层面提出了具有高度仿生特征的思路。将提取自 THP-1 巨噬细胞和 ACE2-293T 细胞的膜以 1:1 的蛋白质量比例融合,形成了杂化细胞膜(2TM)。这一外层膜保留了天然受体蛋白,包括 ACE2、IL6ST 和 CD116,使得机器人同时具备与 SARS-CoV-2 假病毒结合以及清除 IL-6 和 GM-CSF 等关键炎症因子的能力。在运动机制上,研究人员利用天然磁螺菌 AMB-1 作为引擎,其体内磁小体链能对外加旋转磁场迅速响应,从而赋予机器人方向可控且速度较高的运动能力。在药物负载方面,团队将具有抗炎作用的姜黄素包裹于人血清白蛋白纳米粒中,作为治疗因子嵌入系统。为了将上述各部分高效组装为一体,研究人员利用点击化学,通过代谢标记在细胞膜表面引入叠氮基团,在细菌表面修饰 DBCO 基团,借助高效的化学反应实现了稳定结合,形成最终的 AR 微型机器人。
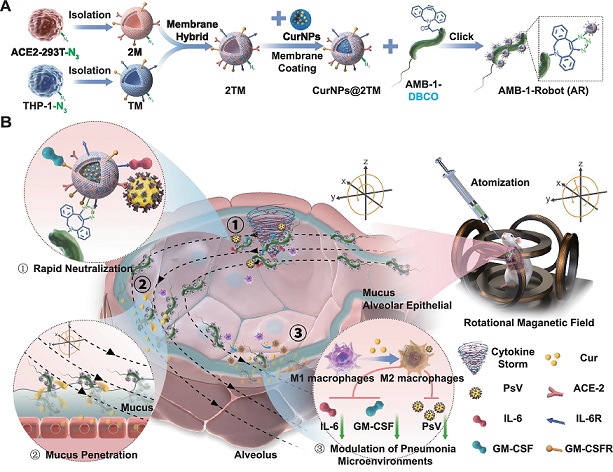
图 | 仿生磁细菌微型机器人的设计与功能
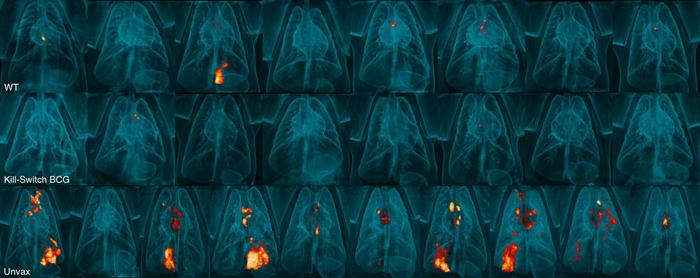
在功能验证中,研究人员通过体外实验首先确认了该系统在磁场驱动下的可控运动能力。在模拟肺液环境中,AR 能在旋转磁场作用下实现高速可控的运动,其速度最高可达 38 μm/s,并能按照外部指令完成复杂轨迹的运动。进一步在小鼠模型中,研究人员发现,与传统被动递送的纳米颗粒相比,AR 在磁场辅助下的肺部滞留时间显著延长,由不足 48 小时提升至 72 小时,且药物在病灶区域的富集量提高了三倍。组织切片分析进一步证实,AR 能够穿透黏液屏障并抵达肺泡上皮,从而增强局部药物浓度和作用时间。
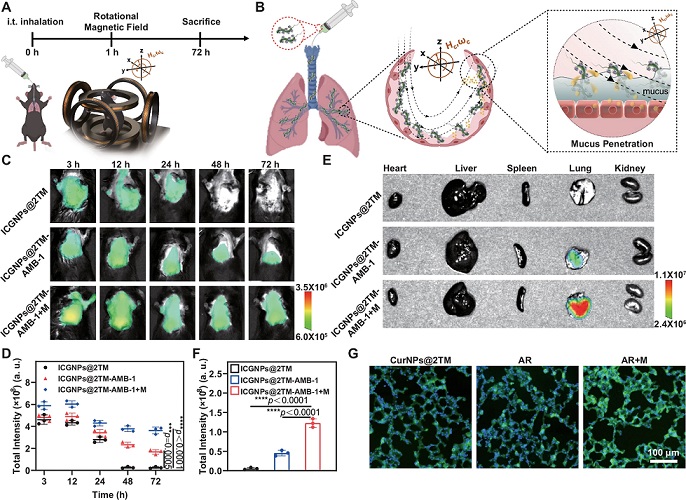
图 | AR 在小鼠肺部的分布与滞留效果
在治疗效果方面,AR 展现了多重协同作用。其外层膜通过受体作用能够清除超过 90% 的病毒颗粒,并中和约 83% 的 IL-6 和 76% 的 GM-CSF,从源头减弱了炎症风暴的触发。与此同时,磁驱动促进其在炎症区域的富集并提升姜黄素的释放效率,使药物作用更加集中。进一步的免疫学分析显示,AR 不仅降低了炎症相关因子的水平,还显著促进了巨噬细胞从 M1 型向 M2 型的极化,M2 比例提升至 41.7%,从而实现了免疫微环境向抑炎修复状态的转变。在动物模型中,这种免疫调控与药物递送的结合显著降低了肺组织损伤评分,减少了肺水肿,证明其在多维度上改善了病理表现。
安全性评价同样为该系统的临床潜力提供了有力支持。细胞毒性实验表明,AR 与对照组相比无显著差异,细胞存活率超过 90%。在动物实验中,血清学检测显示肝肾功能指标与对照组无差异,主要脏器的病理切片未见明显损伤。作为动力来源的 AMB-1 细菌在 72 小时内被肺部代谢清除,且未出现向其他器官迁移的情况。这些结果共同表明,AR 不仅具有良好的治疗效果,也具备较高的安全性和可清除性。
整体来看,这项研究通过合成生物学与微纳机器人技术的融合,成功构建了一个能够执行多重任务的生物混合平台,填补了肺炎治疗中主动靶向与微环境调控的空白。其模块化设计意味着该平台具有较强的可扩展性,通过更换不同来源的细胞膜,可以实现针对其他病原体或炎症因子的特异性靶向;通过调整药物负载,可以拓展至慢性阻塞性肺疾病、哮喘乃至肺癌等其他呼吸系统疾病的治疗。展望未来,如果与超声或 MRI 等影像技术结合,AR 有望在体内实现实时导航与反馈控制,进一步增强精准性与可操作性。这项成果不仅为肺炎治疗提供了新的解决方案,也为微纳机器人在临床中的应用开辟了前景。
参考链接:
1.Zhang, L., Chen, Z., Ran, H. et al. Biomimetic magnetobacterial microrobots for active pneumonia therapy. Nat Commun 16, 7856 (2025). https://doi.org/10.1038/s41467-025-63231-6
免责声明:本文旨在传递合成生物学最新讯息,不代表平台立场,不构成任何投资意见和建议,以官方/公司公告为准。本文也不是治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。




































































































































































































安各洛(深圳)生物科技有限公司 版权所有